实验室王琳淇研究团队在新生隐球菌和格特隐球菌致病性差异调控的分子进化基础研究方面取得进展

一、导读
新生隐球菌和格特隐球菌是重要的侵袭性人类病原真菌,二者亲缘关系紧密但临床特征有别。本研究对决定它们致病性差异的分子进化基础进行了系统性揭示,确定了Hcm1-Srx1抗氧化通路在其中的关键贡献。
二、背景介绍
新生隐球菌和格特隐球菌是担子菌门最为重要的侵袭性人类病原真菌,其平均感染病死率超过20%。二者在系统发育上关系密切,具有极为相似的无性和有性生活周期,因此曾一度被认为属于同一物种。但两者在感染特征上存在明显不同:新生隐球菌为真菌脑膜炎头号病原体,但肺部感染能力相对较弱;相比而言,格特隐球菌较易引起严重的隐球菌肺炎。这些不同暗示了决定两者致病性的分子与调控基础具有差异。然而,导致差异的因素尚不清楚。
三、主要科学发现
本研究揭示了一个功能未知的forkhead家族转录因子Hcm1在新生隐球菌和格特隐球菌肺部感染过程中扮演了截然不同的角色。通过逐一评估24种物化压力条件下Hcm1对于两种病原菌生存能力的影响,证明了Hcm1介导的毒力调控差异与其在不同病原菌中抗氧化能力上的差别高度相关。通过解析Hcm1的作用机制,发现内源性硫过氧化物还原因子Srx1作为Hcm1的关键靶点,直接影响了其介导的毒力和氧化应激调控差异。在此基础上,我们进一步比较了新生隐球菌和格特隐球菌的不同临床菌株的抗氧化和肺部感染能力,揭示了两种病原菌在抗氧化能力上的差别可能是导致其肺部感染特征不同的重要原因。
1. 鉴定关键的转录因子Hcm1介导新生隐球菌和格特隐球菌的毒力调控差异。
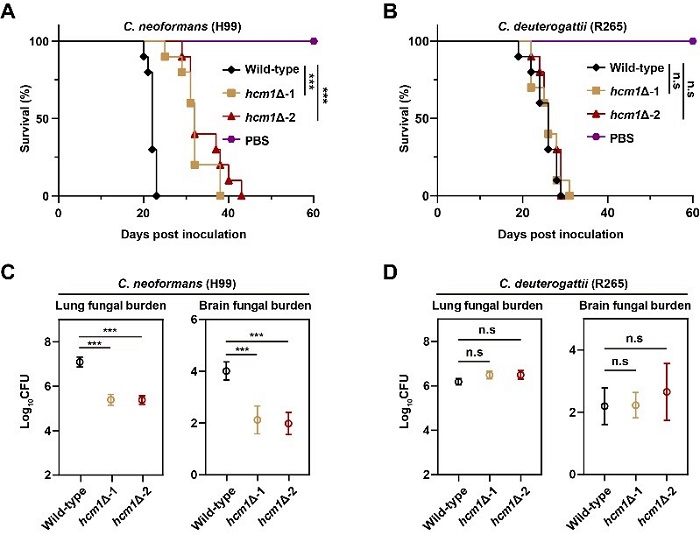
图1. Hcm1促进新生隐球菌的致病性,而不影响格特隐球菌的毒力。
(A) 新生隐球菌Hcm1的缺失显著降低其致病能力。
(B) 格特隐球菌Hcm1的缺失不影响其致病性。
(C) Hcm1缺失显著降低新生隐球菌在肺部和脑部中的菌载量。
(D) Hcm1缺失对于格特隐球菌在肺部和脑部中的菌载量无影响。
2. Hcm1对新生和格特隐球菌的毒力调控差异与其对抗氧化胁迫的贡献高度相关。
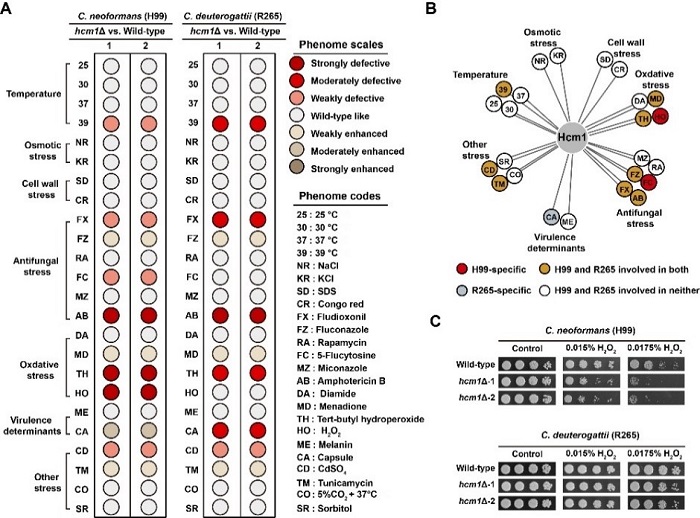
图2. Hcm1在新生隐球菌中,对抗氧化胁迫的贡献强于格特隐球菌。
(A) 24种物化压力胁迫,Hcm1缺失突变株相对于对于野生型的半定量表型。
(B) Hcm1在新生和格特隐球菌种中的表型相关性分析。
(C) Hcm1缺失突变株与野生型在H2O2条件下的生长表型差异。
3. Srx1作为Hcm1关键的抗氧化靶点介导毒力调控差异。
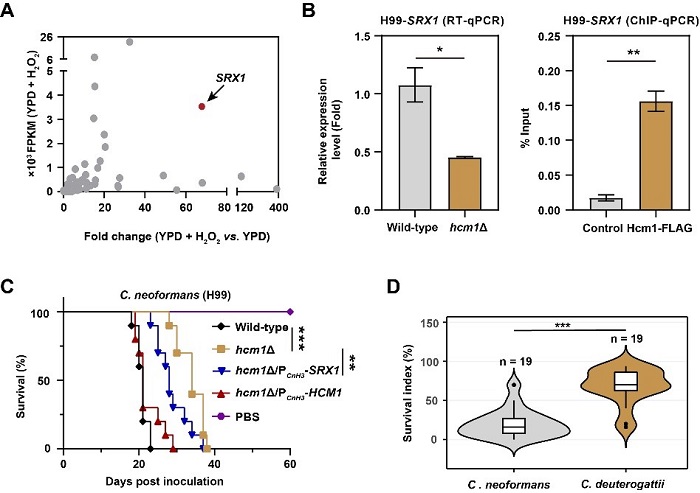
图3. Hcm1在新生隐球菌中,对抗氧化胁迫的贡献强于格特隐球菌。
(A) Hcm1下游靶点SRX1的转录水平在双氧水条件下被高度诱导。
(B) RT-qPCR及ChIP-qPCR表明SRX1受Hcm1的直接调控。
(C) 过表达SRX1在很大程度上恢复Hcm1缺失导致的毒力缺陷。
(D) 新生隐球菌的临床菌株抗氧化能力显著弱于临床格特隐球菌菌株。
四、总结展望
本研究针对担子菌门最为重要的两个侵袭性病原真菌—新生隐球菌和格特隐球菌,旨在理解决定它们肺部感染差异的关键因子。本研究揭示了两者在抗氧化能力上的差别可能在其中扮演了关键的角色,推动了对这两种亲缘关系密切的真菌病原体毒力进化途径与分子基础的理解,为新型抗隐球菌药物的开发提供了一定的理论基础。

Ke, W, Xie, Y, Hu, Y, Ding, H, Fan, X, Huang, J, et al. A forkhead transcription factor contributes to the regulatory differences of pathogenicity in closely related fungal pathogens. mLife. 2022; 1:79-91
五、作者信息
1. 论文作者(第一作者):
作者姓名:柯维鑫

作者单位:中国科学院微生物研究所
作者职称:无
作者简介:柯维鑫,中国科学院微生物研究所在读博士,本科毕业于西南大学,作为第一作者在mLife或共同作者在Nature Microbiol、Annu Rev Microbiol、Sci China Life Sci等专业期刊发表论文;曾获得中国科学院微生物研究所“劲牛”、“牛栏山”等奖学金及中国科学院大学优秀学生干部、三好学生荣誉称号;第十一届全国微生物学青年学者学术研讨会研究生论坛一等奖。
2. 论文作者(通讯作者):
作者姓名:王琳淇

作者单位:中国科学院微生物研究所
作者职称:正高级
作者简介:王琳淇,博士,研究员,真菌学国家重点实验室副主任,国家自然科学基金委“优秀青年基金”获得者(2016),中科院引进国外杰出人才计划“优秀”(2019),中科院创新交叉团队负责人(2020), 入选Faculty Opinions (F1000)的Faculty member(2021)。兼任中国菌物学会遗传与分子生物学专业委员会主任,中国遗传学会微生物遗传专业委员会副主任,中国微生物学会普通微生物学专委会副主任、中国微生物学会真菌学专委会副主任等;任Innovation、mLife、Front Cell Infect Microbiol、Mycology等期刊编委。致力于人类环境病原真菌环境适应、感染和耐药的研究,作为通讯作者在Nature Microbiol、Annu Rev Microbiol、eLife、PLoS Pathog、PLoS Genet、Curr Opin Microbiol、Microbiol Spectr、Sci China Life Sci、mLife等专业期刊发表论文。



 京公网安备 11010502044263号
京公网安备 11010502044263号